비경구 투여 바이오 의약 제제와 관련하여 단백질 응집체 형성은 면역원성 증가 가능성의 측면에서 중요한 문제입니다. 따라서 규제 기관에서는 바이오 의약 제제 제조 업체들이 단백질 치료제의 전체 사용 수명에 걸쳐 그 내에 존재하는 미립자를 모니터링하고 필요한 경우 그 수준을 줄일 것을 요구하고 있습니다. 면역원성은 다양한 메커니즘으로 유발될 수 있지만 비단백질 물질에 의한 오염이 하나의 원인일 수 있는 것으로 알려져 있습니다. 주사기를 통해 투여될 때, 단백질 응집체와 오일 방울을 구분하기가 어렵다는 점 때문에 비경구 약물에 들어 있는 실리콘 오일은 연구자들의 관심을 끌어왔습니다. 단백질 응집체와 더불어 비생물학적 오염원이 응집체 크기 증가의 핵점(nucleation point)으로 작용할 수 있다는 문제도 있습니다. 따라서 입자의 크기를 분석하는 것만으로는 충분하지 않습니다.
바이오 의약품 산업에 관한 미국 FDA 지침에는 "천연 재료로 만든 제품의 경우 다른 성분, 단백질, 비단백질 등의 물질에 대해서도 평가해야 한다.”(1)라고 명시되어 있습니다. Archimedes 시스템에 적용된 공명 질량 측정(RMM) 기술은 캔틸레버를 통과하는 입자의 부력을 측정하여 완충액에 들어있는 것과 다른 밀도의 입자를 검출해 낼 수 있도록 합니다. 이를 통해 Archimedes는 단백질처럼 완충용액보다 밀도가 높은 경우 음의 피크(음전위)를 실리콘 오일처럼 밀도가 낮은 입자는 양의 피크(양전위)로 측정되어 각각의 부유 입자들을 구분할 수 있습니다. 이 응용 노트에서는 Archimedes가 어떻게 단백질 미립자가 형성되는 것을 검출하고는 정량화하는지에 관하여 설명하고 전단 응력에 의해 주입된 실리콘 오일을 예로 듭니다.

|
소혈청알부민(BSA)(Sigma Aldrich, 영국 풀)을 최종 농도 20mg/mL로 준비하고 0.2µm 주사기 필터로 여과하였습니다. 이때 분산매는 증류수입니다. 준비한 샘플을 전단 응력을 가하기 전과 후에 각각 분석하였습니다. BSA 용액을 2mL 주사기와 여기에 부착된 2게이지의 3 주사 바늘로 반복해서 주사하는 방식으로 전단 응력을 유도하였습니다. Archimedes 공명 질량 측정(RMM) 시스템에 마이크로 센서를 장착하여 분석하였습니다. 샘플 테스트를 시작하기 전에 마이크로 센서를 증류수로 헹구고 1µm 라텍스 비드와 중수소로 치환된 증류수를 사용해 보정하였습니다. 0.1µL로 샘플 부피를 한정하고 검출 한계를 0.02Hz로 설정한 상태에서 양전위 및 음전위 부유 입자를 검출하였습니다.
전단 응력이 단백질 응집체 형성과 실리콘 오일 유도에 미치는 영향을 Archimedes 시스템으로 분석하였습니다. 측정 결과는 아래와 같습니다.
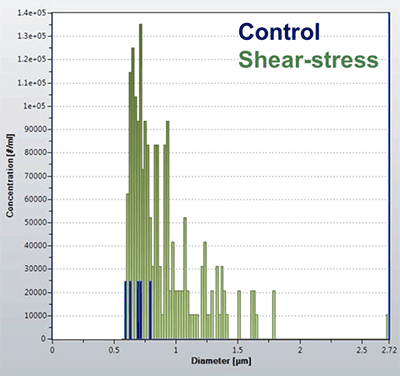
주사기를 이용해 유도된 전단 응력을 가하기 전과 후에 RMM으로 미립자를 정량화하였습니다. 이 데이터는 그림 2에 있습니다. 주사기로 응력을 가하기 전에 Archimedes 시스템에 의해 검출된 입자의 수는 매우 적었으며 이는 해당 샘플의 순도가 적절하며 대형 단백질 응집체가 거의 포함돼 있지 않다는 것을 의미합니다. 이것은 샘플을 여과했기 때문에 가능한 결과이며 동시에, 적용한 기술의 노이즈 기준선이 낮아 고순도 샘플에 대한 정밀 분석이 가능하다는 증거이기도 합니다. 전단 응력을 가한 후에는 검출된 입자의 수가 유의하게 증가였으며 입자 크기는 500nm에서 1700nm 범위였습니다. 유도된 응력 유형에 대한 반응과 관련하여 입자 크기 분포는 중요한 데이터입니다. 이러한 데이터는 각기 다른 응력 조건을 비교함으로써 바이오 의약품의 전반적인 양상을 분석하고 파악하는 데 이용할 수 있습니다.
|
생물공정이 단백질의 성질 변화에 미치는 영향을 이해하는 것은 의약 제품에 대한 지식의 확대와 제조 매개 변수의 구상이라는 측면에서 매우 중요합니다. 규제 요건을 충족하기 위해서는 제조 공정에 사용된 물질이 결과물에 미치는 영향을 평가하여 해당 물질이 제품의 최종 품질에 영향을 주지 않도록 해야 합니다. 바이오 의약품은 각각의 단백질 및 제형의 특성과 더불어 여과 및 추출 가능 성분의 유형에 따라 제품과 접촉하는 요소들의 구성이 다양하기 때문에 물질들의 적합성이 달라질 수 있습니다. 따라서 제품 접촉 요소의 영향을 서로 비교해 볼 필요가 있습니다. 서로 다른 2개 제조사에서 만든 주사기로 전단 응력을 가해 유도한 미립자의 특성을 RMM을 통해 비교하였습니다. 이 데이터는 그림 3A에 있습니다.
방법 부분의 설명과 같이 서로 다른 2개 제조사의 1mL 주사기를 사용해 전단 응력을 유도하였습니다. 그림 3A의 데이터에 따르면 1번 제조사의 주사기로 유도한 미립자의 개수(빨간 막대)가 2번 제조사 주사기로 유도한 입자 수(파란 막대)보다 훨씬 많았습니다. 이 데이터를 통해 단백질이 2번보다 1번 제조사의 주사기가 더 적합한 것을 알 수 있습니다.

|
부유 질량을 기초로 실리콘 입자를 단백질 응집체와 구분해 내는 기술은 Archimedes RMM 시스템의 큰 장점 중 하나입니다. 이전 실험에서 나온 양전위 입자 질량 데이터가 그림 3B에 제시되어 있습니다. 이 데이터를 통해 테스트에 사용한 두 가지 주사기 내에 실리콘 오일이 존재함을 알 수 있습니다. 단백질 응집체가 음의 주파수 전이를 유발하는 데 반해 물에서 양전위 부력을 갖는 실리콘은 양의 주파수 전이를 유발합니다(그림 3C). 이 기술을 이용하면 단백질 자체에 부정적인 영향을 주거나 약물 투여 후 면역원성 증가의 원인이 될 수 있는 실리콘 오일 성분을 정량적으로 분석할 수 있습니다. 그림 3의 데이터에 따르면 단백질 샘플에 대해 반복적으로 전단 응력을 가했을 때 1번 제조사의 주사기(빨간 막대)가 유도하는 오일이 유의하게 더 많다는 것을 알 수 있습니다. 실리콘 오일 농도의 증가는 해당 주사기를 통해 검출되는 단백질 응집체 수 증가의 원인일 수 있습니다. 실리콘 오일 성분을 검출하고 정량화할 수 있으면 제품의 성질을 보다 구체적으로 파악할 수 있으며 따라서 해당 제품의 분해 과정에 관해 더 잘 이해할 수 있습니다.
FDA에서 권장한 바와 같이 단백질 응집체와 비단백질 물질을 구분해 낼 수 있는 능력은 바이오 의약품의 안정성에 대한 연구와 모니터링에 있어 중요한 역할을 합니다. 이 응용 노트에서는 전단 응력에 의해 유도된 단백질 응집체와 실리콘 오일을 정량화하는 Archimedes 시스템의 능력에 대해 설명합니다. 이러한 분석 데이터는 의약 제품의 안정성과 면역원성 그리고 생물공정이 결과물에 미치는 영향을 이해하는 데 있어 매우 유용한 정보입니다. 또한 단백질 응집체와 실리콘 오일을 구별함으로써 제품 연구 과정에서 접하게 되는 어려운 문제들을 보다 효과적으로 해결할 수 있습니다. 간단한 분석으로 실리콘 오일을 어떤 문제의 잠재적인 근본 원인(3)에 포함시키거나 배제함으로써 가장 가능성이 높은 원인을 찾아내는 데 더 많은 노력을 집중할 수 있습니다. 현재의 분석 장비로는 면역원성을 이해하는 데 있어 중요한 크기인 0.2 ~ 5µm 범위의 입자를 정량화하는 데에 어려움이 많은데, Archimedes를 이용하여 이를 포함한 광범위한 입자 크기 범위의 단백질을 정량적으로 분석할 수 있습니다[1].
결론적으로, Archimedes RMM 시스템은 미립자의 형성 및 실리콘 오일과 같은 비단백질 오염 물질의 존재와 관련하여 바이오 의약품에 대한 매우 중요한 정보를 제공합니다.
Guidance for Industry: Immunogenicity Assessment for Therapeutic Protein Products (2013): FDA
Code of Federal Regulations; CFR21, Part211.65
Characterization and Quantitation of Aggregates and Particles in Interferon-β Products: Potential Links Between Product Quality Attributes and Immunogenicity (2013): J. Pharm. Sci. (102) p.915