Warum ist die Nähe entscheidend? – Viscotek GPC-System
Einführung
Derzeit wird beim Messen der Molekularmasse in GPC/SEC (Gelpermeationschromatographie/Größenausschluss-chromatographie) Experimenten häufig ein Laserstreulichtdetektor verwendet.
Molekularmassewird direkt über das LS (Streulicht) Detektorsignal gemessen, was es überflüssig macht, die Elutionsmenge mit Polymeren oder Standardproteinen anzugleichen. Viele Anwender bevorzugen dies, da die gemessene Molekularmasse mit dem Polymertyp und der Struktur unabhängig ist.
Aus diesem Grund wird die Molekularmasse, die mit GPC-LS gemessen wird, als absolute Molekularmasse bezeichnet. In der Tat ist bei allen GPC-LS Detektoren eine Kalibrierung erforderlich, da die meisten der derzeit verwendeten LS Detektoren ihre Daten extrapolieren oder kalibrieren, so dass die tatsächlichen Werte nicht absolut sind.
Diese Anwendungshinweise erklären die Theorie zu dieser Problematik und erläutern, ob LALS (Low Angle Light Scattering) die einzige LS-Technik ist, die den Streuwinkel des Lichts proportional zur Molekularmasse direkt misst.
Die Theorie des Lichtstreuens
Zuerst ist es wichtig, die Beziehung zwischen den gemessenen Werten (Intensität des Streulichts) und den gewünschten Ergebnissen (gewichtetes Molekularmittel) zu verstehen. Diese Werte stehen in der bekannten Raleigh-Gleichung miteinander in Verbindung.
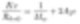
Dabei steht R=o für die Streuintensität bei 0 Grad, Mw für die durchschnittliche Molekularmasse, c für die Konzentration der Lösung, und K repräsentiert den optischen Konstantenwert, der dn/dc bedeutet, während A2 den zweiten Virialkoeffizienten darstellt.
Bei niedrigen Konzentrationen (z.B. bei typischen GPC-Bedingungen) kann dieser Einfluss aufgrund der sehr geringen Konzentration vernachlässigt werden. Dadurch wird die Gleichung wie folgt vereinfacht.

Diese vereinfachte Gleichung ermöglicht es, Mw direkt von der Streuwert zu bestimmen. Jedoch ist es wichtig zu verstehen, dass diese Gleichung für die Streularithmetik bei 0 Grad (z.B. 0°) relevant ist.
Aufgrund des einfallenden Laserstrahls ist es jedoch unmöglich, das Streulicht bei 0 Grad zu messen, so dass das Streulicht bei mehreren anderen Winkeln gemessen werden muss (Abbildung 1). Dabei variiert die Menge des gestreuten Lichts je nach Streuwinkel und der zu messenden Molekülgröße erheblich, was den Prozess
kompliziert.

Nur wenn die Molekülgröße sehr klein ist, kann dieser Winkelabhängigkeitseffekt vernachlässigt werden. Bei Molekülgrößen über 12 nm treten Probleme mit der Lösung auf. (1)
Laut dieser Theorie gibt es grundsätzlich drei Lösungen.
1. Mehrwinkellichtstreuung (MALS).
Gemessen wird das Streulicht bei mindestens zwei Winkeln und die Daten werden auf 0 Grad extrapoliert.
2. 90 Grad Lichtstreuung/Viskosität (RALS/Viskosität).
Das Streulicht wird bei 90° gemessen und die Werte durch Viskositätsmessungen für 0° korrigiert.
3. Niedrige Winkellichtstreuung (LALS).
Gemessen wird bei einem Winkel nahe 0°, bei dem die Winkeleffekte vernachlässigbar sind, und eine Kalibrierung nicht erforderlich ist.
Hunderte von Geräten, die MALS oder RALS/Viskosität verwenden, sind derzeit weltweit im Einsatz, wobei keiner dieser Geräte die Molekularmasse direkt misst.
Dieser Mehrwinkelansatz hängt immer von der Datenextrapolation ab, während der RALS-Ansatz einen Viskositätskorrektor zur Datenerweiterung bei großen Molekülen erfordert.
Historisch betrachtet wird der LALS-Ansatz als die einzige absolute Methode angesehen, da er nach der ersten Kalibrierung die Molekularmasse direkt misst und wie beim Mehrwinkelansatz keine Schätzungen oder datenmanipulierenden Maßnahmen erforderlich sind.
Kommerzielle LALS-Detektoren basieren auf dem Chromatix KMX-6, das von den späten 1970er bis in die späten 1980er Jahre produziert wurde. In den 1990er Jahren jedoch wurde kein einziger LALS-Detektor produziert.
Erst 2001 stellte Viscotek einen neuen LALS-Detektor vor, der GPC-LS-Anwendern die Möglichkeit bot, die absolute Molekularmasse selbst zu messen.
Probleme des Mehrwinkelansatzes
Mehrwinkelgeräte beruhen auf der Messung des Streuens bei mindestens zwei Winkeln, um die Werte auf 0 Grad zu extrapolieren. Viele Benutzer nehmen fälschlicherweise an, dass die erhaltenen Werte die absolute Molekularmasse darstellen.
Tatsächlich erfordert jedes MALS-Gerät eine Kalibrierung, die Molekularmasse wird nicht direkt, sondern durch Datenextrapolation ermittelt.
Dies ist der große Schwachpunkt des MALS-Verfahrens. Für die Extrapolation gibt es verschiedene Arten von Datenplots oder Anpassungsoptionen – welche ist die richtige für Ihre Probe? Debye? Zimm? Berry? Bei kleinen Molekülen ist die lineare Anpassung am genauesten, doch für größere Moleküle können sich die erforderlichen Anpassungen stark unterscheiden (2).
Bei Molekülen, die größer als 45 nm sind, neigt der Datenplot zur Kurvatur, und das extrapolierte Molekulargewicht hängt vom gewählten Anpassungsfit ab. Bei Proben, die sowohl kleine als auch große Moleküle umfassen, kann die Reihenfolge der Anpassung erheblich beeinflussen.
Ein weiteres Problem mit der Mehrwinkelapproach ist das Fehlen von Daten in dem kritischen Bereich mit niedrigen Winkeln. Multiangle-Detektoren wurden entwickelt, um Daten bei verschiedenen Winkeln zu sammeln, was bedeutet, dass sie keine genauen Daten bei tatsächlichen Low angles sammeln können.
Dies erschwert es, eine genaue Messung der Molekularmasse zu erhalten. Die Extrapolationspräzision (Fit-Eignung) wird durch die Nähe der niedrigwinkeligen Datenpunkte zu 0 und die Signalqualität bestimmt. (3)
Niedrige Winkellichtstreuung (LALS)
Die fortgeschrittene LALS-Approach misst die Streulichtintensität so nah wie möglich an 0° (hier bei 7°), um alle Extrapolations- und Datenanpassungsprobleme zu vermeiden.

Abbildung 2 ist eine modellierte Darstellung des optischen Pfades im Detektor. Diese effiziente Gestaltung trennt den einfallenden Strahl effektiv vom Lichtstreuensignal (4). Das Ergebnis ist eine hervorragende Signal-Rausch-Verhältnis bei 7°.

Abbildung 3 vergleicht das Signal-Rausch-Verhältnis für niedrigmolekulare und hochmolekulare Polymere bei 90° (RALS) und 7° (LALS).
Abbildung 3a zeigt, dass beide Detektoren bei Proben niedriger Molekülmasse, unabhängig vom Streuwinkel, die gleichen Ergebnisse liefern. Das Chromatogramm vergleicht direkt das Signal-Rausch-Verhältnis bei 90° (RALS) und LALS, wobei LALS ein überlegenes Signalanzeige-Rausch-Verhältnis bietet.
Die Bedeutung der direkten LALS-Messung wird deutlich beim Analysieren großer Moleküle wie Polysaccharide. Solche Moleküle weisen eine starke Winkelabhängigkeit des Streulichts auf (siehe Abbildung 3b), was bei RALS- und insbesondere beim Mehrwinkelansatz erhebliche Probleme verursacht.

Durch die direkte Messung bei 7° kann eine exakte Berechnung der Molekularmasse erfolgen, ohne dass Extrapolation oder Datenanpassung erforderlich ist. Abbildung 4 zeigt die Ergebnisse der Messung von Hyaluronsäureproben mit der LALS-Methode (5).
Fazit
Dank der neuesten LALS-Detektoren können GPC/SEC-Labore die Molekularmasse der Proben präzise messen.
LALS verhindert Probleme, die im Zusammenhang mit Datenextrapolation oder Datenanpassung auftreten können. Das neue LALS-Produkt ist kompakt und leicht zu handhaben und kann problemlos in integrierte Multi-Detektor-Systeme mit Viskosimeter integriert werden (6), wodurch Molekularmasse und Molekülstruktur gleichzeitig bestimmt werden können (7, 8).
Dies überholt das frühere Denken, dass verschiedene Winkel besser sind. Tatsächlich ist es beim Messen der Streulichtintensität besser, je näher man dem Ziel ist.
{{ product.product_name }}
{{ product.product_strapline }}
{{ product.product_lede }}
