最佳實踐:利用等溫滴定量熱法研究結合相互作用 – 第1部分
以下是使用 MicroCal PEAQ-ITC、VP-ITC 和 ITC200 系統進行傳統結合實驗的幾個最佳實踐。
樣品要求:
-
- 按照慣例,在等溫滴定量熱儀(ITC)細胞中的“高分子”是生物分子,而“配體”是ITC注射器中的生物分子。這些可以是任何互相作用的分子(蛋白質、核酸、小分子抑制劑、金屬等)。也可以進行“反向滴定”,使“配體”在注射器中。
- 為了數據分析到一組位點結合模型,“配體”有一個結合位點以及其他常用的ITC數據分析模型。“高分子”可以有任意數量的結合位點。
- 所有樣品應儘可能純淨,以便用於ITC。避免或消除化學和構象上的雜質,因為這些可能影響準確的濃度測定,並可能參與或干擾結合相互作用。
- 為了獲得高質量的ITC數據,必須將兩個生物分子匹配在所需的緩衝液中,以避免因緩衝液不匹配導致的熱量變化。

- ITC的緩衝液:
- 使用能夠保持生物分子溶解度和穩定性的緩衝液,包含任何結合所需的鹽、輔助因子和添加劑。
- 作為初始點,可以使用其他結合研究中使用的相同緩衝液。
- ITC與pH2-pH12之間的水性緩衝液兼容。確保緩衝液濃度足夠在存在生物分子的情況下保持pH值。
- 如果緩衝液中含有甘油(或其他黏性成分),保持甘油濃度低於20%(v/v),以避免在ITC池和注射器中產生氣泡。
- 如果緩衝液中含有表面活性劑或洗滌劑,保持表面活性劑濃度低於其臨界膠束濃度(CMC),除非您正在研究ITC中的膠束。
- 如果需要還原劑,我們推薦使用TCEP或2-巰基乙醇。不建議使用二硫蘇糖醇。
- 如果配體需要DMSO以溶解,確保在結合夥伴中具有相同的最終DMSO濃度。ITC結合研究建議的上限是10%DMSO。
- 如果需要使用其他有機溶劑,檢查儀器的技術文獻或諮詢您所在地區的Malvern Panalytical支持團隊,獲取建議和ITC系統的化學兼容性。
樣品體積:
- 請參閱表1。這些是按照推薦協議所需填充ITC池和注射器的建議體積,且無需加入氣泡。
樣品濃度:
- ITC池中的起始高分子濃度通常由“C參數”或“sigmoidocity係數”確定,其計算公式為:
C= N[M]T/KD - [M]T是ITC細胞中的高分子濃度,而N是化學計量。為獲得合理的ITC結合等溫圖,最佳範圍為5 < C < 500。在很多情況下,當C介於1和1000之間時,您可以從ITC結合曲線中獲得一些有用的數據。
- 對於1:1的結合,開始時使用ITC注射器中比ITC細胞中高分子濃度高10倍的配體濃度。
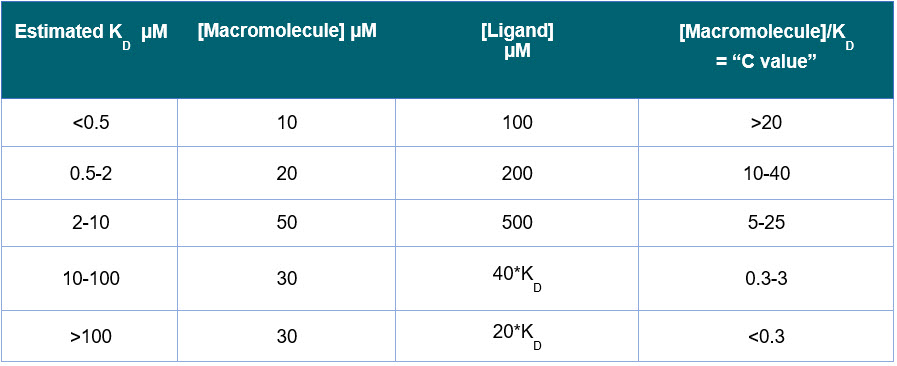
- 如果估計的KD,並且是1:1的結合,請使用表2中的指南。假設存在合理的熱量變化和結合焓,這些濃度範圍應該可以提供結合曲線。
- 如果KD未知,請嘗試ITC池中20 μM樣品和ITC注射器中200 μM樣品。
- ITC池中的最低濃度:5-10 μM
- ITC注射器中的最低濃度:50 μM
相關內容:
- 等溫滴定量熱法:理論與實踐
- MicroCal PEAQ-ITC實驗的實用技巧
- ITC解決結合相互作用的複雜性 – 充分利用您的ITC數據
- 生物分子:相互作用分析中的樣品和數據質量 – 同一枚硬幣的兩面
- 不要丟掉你的“壞”N值ITC數據
- 結合親和力的黃金標準
以前的文章:
{{ product.product_name }}
{{ product.product_strapline }}
{{ product.product_lede }}


