Constante de dissociation
Mesure cinétique précise des événements de liaison
Mesure cinétique précise des événements de liaison
La constante de dissociation est un paramètre cinétique utilisé lors de la mesure des interactions intermoléculaires et des événements de liaison entre deux molécules ou plus. Le taux d'association (ka) décrit la vitesse à laquelle une molécule se lie à l'autre pour former un complexe et le taux de dissociation (kd) décrit la vitesse à laquelle le complexe se décompose. Ils sont exprimés avec l'unité s-1. Ensemble, ces paramètres déterminent la constante de dissociation à l'équilibre, ou affinité de liaison (KD).
Le graphique ci-dessous présente les résultats de la mesure d'une interaction de liaison. Dans un premier temps, la ligne de base est établie en laissant s'écouler le tampon devant le capteur avec un ligand immobilisé. L'échantillon (analyte) s'écoule ensuite. L'analyte s'associe au ligand pendant la phase d'association, à partir de laquelle la constante d'association peut être calculée. La phase de dissociation commence lorsque la substance du flux passe de l'échantillon au tampon.
Courbe résultant de la mesure d'une interaction de liaison (appelée « sensorgramme »).
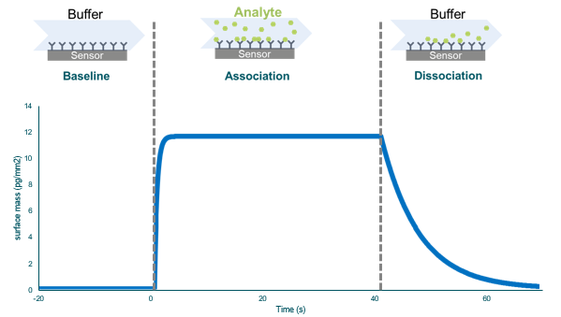
Deux interactions peuvent présenter la même affinité (KD), mais des cinétiques très différentes (ka et kd).
Dans l'exemple ci-dessous, l'interaction représentée par la ligne bleue présente une association et une dissociation rapides, tandis que l'interaction représentée par la ligne rouge présente une association et une dissociation nettement plus lentes.
Ces deux interactions présentent le même rapport kd/ka et donc la même affinité (KD).
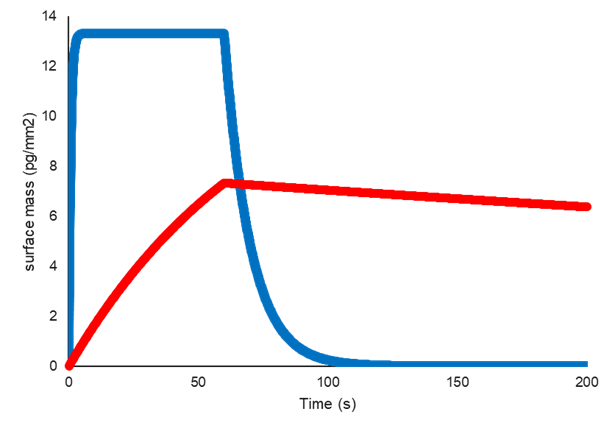
Exemple de deux interactions présentant la même affinité (KD), mais des cinétiques différentes (ka et kd)
Cela signifie que la mesure de l'affinité seule n'est souvent pas suffisante pour déterminer les composés qui mériteraient d'être développés en un médicament. Un chercheur souhaitera probablement obtenir une interaction rapide jusqu'à saturation entre le médicament et la cible, comme dans l'interaction représentée par la ligne bleue.
En pharmacologie, et plus particulièrement dans le domaine de la découverte de médicaments, le taux de dissociation est un paramètre important pour déterminer le potentiel d'un médicament : la durée pendant laquelle un médicament reste dans le complexe (c.-à-d. le médicament avec la cible médicamenteuse) influence son effet sur la cible, c'est à dire, l'efficacité du médicament. C'est pourquoi, dans la découverte précoce de médicaments, les médicaments potentiels sont souvent analysés et classés en fonction de leur taux de dissociation. Le taux de dissociation (kd ou (koff) peut être mesuré à l'aide d'un biocapteur.
Le WAVEsystem est un biocapteur optique qui mesure la constante de dissociation pendant qu'il mesure la cinétique de liaison. Sa haute sensibilité, combinée à sa compatibilité avec les échantillons bruts et à la méthode waveRAPID® qui permet un débit plus élevé, font du WAVEdelta un système particulièrement adapté au criblage du taux de dissociation.