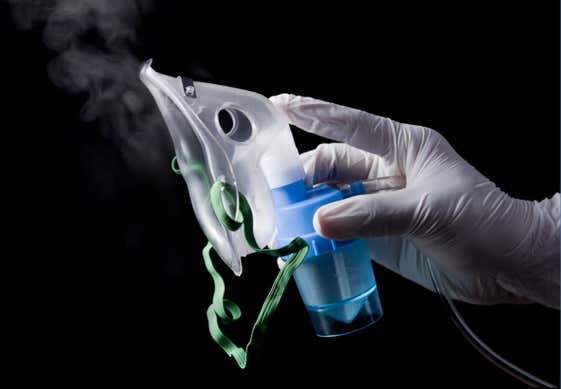
Formulación de productos farmacéuticos inhalados por vía oral y nasal (OINDP)
Análisis fisicoquímico de aerosoles nasales, nebulizadores, inhaladores de polvo seco e inhaladores de dosis medida

UK Pharma Conference - 3 June, Birmingham: learn from & network with thought leaders. Register now
Register nowAnálisis fisicoquímico de aerosoles nasales, nebulizadores, inhaladores de polvo seco e inhaladores de dosis medida

Los productos farmacéuticos inhalados por vía oral y nasal (OINDP, del inglés orally inhaled and nasal drug product), que se utilizan ampliamente para la actividad local, también muestran ser prometedores para la administración sistémica y eficaz de una variedad de tratamientos. La aceptabilidad del paciente, la absorción rápida, la evasión del tubo gastrointestinal y la oportunidad de acceder a la diferenciación del producto son solo algunos de los factores importantes.
Cuando se desarrollan inhaladores o aerosoles, el desarrollo de la formulación y el dispositivo van de la mano. Los cambios realizados para uno afectarán al otro, y viceversa. Por ejemplo, el diseño y la geometría de la boquilla de pulverización afectan el esfuerzo de la suspensión y, por lo tanto, la distribución de las gotas de pulverización. Del mismo modo, un cambio de excipiente puede afectar la viscosidad de la formulación y la eficiencia con la que se puede bombear a través de la boquilla de pulverización. Esto es fundamental, ya que la distribución del tamaño de la gota influye en la ubicación en la que el medicamento se deposita en las vías respiratorias y, por lo tanto, afecta su biodisponibilidad y velocidad de acción.
Las soluciones de análisis fisicoquímico de Malvern Panalytical lo ayudan a entender el impacto de su formulación y las decisiones del proceso sobre el producto farmacéutico final, lo que lo guía hacia el éxito.

Cuando elige sus excipientes, existen varias consideraciones que pueden afectar la formulación o, incluso, el medicamento final. Los excipientes, como los polímeros, se usan a menudo para modular la viscosidad de una suspensión o solución. Por lo tanto, a menudo, pueden influir en la facilidad de bombeo o procesamiento de la suspensión, y en el caso de los aerosoles nasales o los nebulizadores pueden afectar directamente la distribución del tamaño de las gotas de pulverización. La distribución del tamaño de partículas del portador del medicamento, como la lactosa en inhaladores de polvo seco, es fundamental para la llevar el medicamento a los pulmones y, a veces, la forma de las partículas de los excipientes y API puede afectar la forma en que interactúan y fluyen durante el procesamiento.
Malvern Panalytical cuenta con varias herramientas que se utilizan comúnmente para el análisis de ingredientes o materias primas de distintos proveedores y que también se pueden aplicar para determinar si los diferentes lotes son iguales o diferentes.



Estudios de degradación acelerada de API y excipientes
La difracción de rayos X por método de polvo proporciona información única sobre los cambios en la forma de cristales de fármacos, el tamaño y la morfología del cristalito, así como cambios en las relaciones entre amorfos y cristalinas del API en la formulación durante estudios de esfuerzo acelerados para evaluar u optimizar la estabilidad de la formulación.
Desarrollo de procesos y monitoreo de procesos
Nuestras herramientas de caracterización se utilizan con para evaluar la estabilidad de los API y excipientes en una formulación a través de las condiciones de procesamiento a fin de garantizar que los parámetros del proceso estén controlados y optimizados para que el producto farmacéutico final cumpla con los atributos críticos de calidad (CQA) requeridos.






En cualquier proceso, es posible que se necesiten cambios. Dentro de la industria farmacéutica, los ejemplos podrían incluir un cambio en el proveedor de un excipiente o API, un cambio de una maquinaria, un movimiento de un producto entre plantas de fabricación o un cambio menor en la composición de la formulación. Todos estos cambios se deben controlar para que no afecten al producto farmacéutico final.
Las soluciones fisicoquímicas de Malvern Panalytical se utilizan con regularidad para ayudar con la evaluación de comparabilidad a fin de comprobar los cambios en un producto cuando se ha producido un cambio en el proceso utilizado para crearlo. Además, nuestras tecnologías también se utilizan para mostrar bioequivalencia in vitro entre los productos de referencia y de prueba cuando se desarrollan genéricos. Estas pruebas pueden demostrar que la combinación del producto y dispositivo genérico ofrece el mismo medicamento de la misma manera que el producto innovador, lo que puede reducir drásticamente la cantidad de pruebas clínicas requeridas y acelerar la llegada al mercado de un producto farmacéutico genérico.